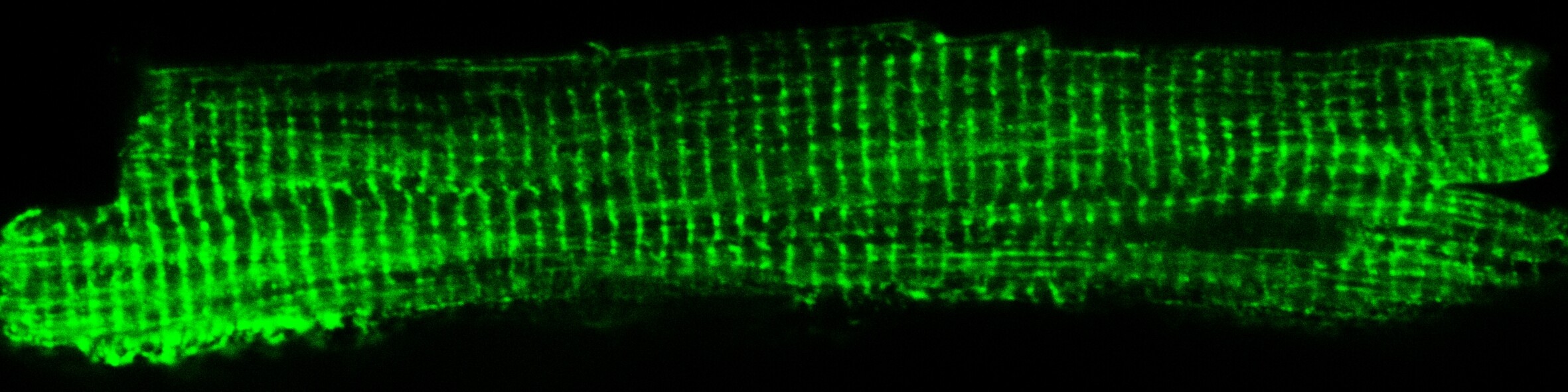
Neue Erkenntnisse zur Herzschwäche – UMG-Herzforscher entwickeln Biosensor zur Darstellung von Herzschwäche in Herzmuskelzellen.
Ein neues Verfahren erlaubt erstmals im In-Vivo-Modell die bildliche Darstellung und Messung des Einflusses einer Herzschwäche auf die Herzmuskelzellen. Veröffentlichung in Nature Communications.
Herzforscher an der Universitätsmedizin Göttingen (UMG) haben neue Erkenntnisse zur Herzschwäche (Herzinsuffizienz) und deren Behandlungsmöglichkeiten gewonnen. Mit Hilfe eines speziellen Biosensors ist es ihnen erstmals gelungen, Einblicke in die Zellkommunikation und Signalverarbeitung von an Herzschwäche erkrankten Herzmuskelzellen in lebenden Organismen zu erhalten. Das neue Verfahren liefert wichtige Informationen darüber, welche molekularen Mechanismen bei Herzschwäche in den Herzmuskelzellen wirken und wie die Prozesse die Zellen verändern. Ihre Arbeiten im Sonderforschungsbereich 1002 „Modulatorische Einheiten bei Herzinsuffizienz“ (SFB 1002) an der Universitätsmedizin Göttingen (UMG) sind durch die Deutsche Forschungsgemeinschaft (DFG) gefördert. Die Forschungsergebnisse helfen, neue Behandlungsstrategien zu erkennen. Bestehende medikamentöse Therapien könnten optimiert werden. Die Ergebnisse wurden im April 2015 in der renommierten Fachzeitschrift „Nature Communications“ veröffentlicht.
Herzschwäche (Herzinsuffizienz) ist eine der häufigsten Erkrankungen in Europa. In den letzten zehn Jahren konnten keine grundlegend neuen Therapieverfahren für die Herzschwäche entwickelt werden. Die Lebenserwartung erkrankter Patienten ist deutlich reduziert. Seit 2012 forschen Göttinger Wissenschaftler im Sonderforschungsbereich 1002 „Modulatorische Einheiten bei Herzinsuffizienz“ (SFB 1002) nach innovativen Verfahren für die Behandlung von Herzschwäche.
Bisher wurden spezielle Biosensoren zur Messung und Darstellung von molekularen Prozessen in einzelnen Herzmuskelzellen nur im Reagenzglas eingesetzt. Ob solche Biosensoren überhaupt in einem sogenannten In-Vivo-Model, d.h. im lebendigen Organismus, eingesetzt werden können, war unklar. Die Göttinger Herzforscher konnten zeigen, dass dies möglich ist.
Damit sind die Auswirkungen von Herzschwäche auf die kleinsten Funktionseinheiten, der Herzmuskelzellen, die sogenannten Mikrodomänen, erstmals im lebendigen Organismus bildlich darstellbar und messbar. Vorteil des neuen Verfahrens ist, dass die Messungen in direkt entnommenen lebenden Zellen erfolgen können. Für bisherige Verfahren mussten die Zellen über mehrere Tage unter künstlichen Bedingungen im Labor kultiviert werden. Dies hatte bei den Messungen zu unerwünschten Artefakten geführt, Zellen starben oder veränderten sich in ihrer Form und Struktur.

„Bisher konnten wir nicht mit Gewissheit sagen, wie die Zellkommunikation bei Herzschwäche im lebendigen Organismus beeinträchtigt wird. Nun haben wir die Möglichkeit, diese Prozesse genau unter die Lupe zu nehmen. Wenn wir wissen, was defekt ist, dann können wir es auch besser therapieren“, sagt Prof. Dr. Gerd Hasenfuß, Sprecher des Sonderforschungsbereiches 1002 „Modulatorische Einheiten bei Herzinsuffizienz“ (SFB 1002) und Vorsitzender des Herzzentrums der UMG.
cAMP sensibler Biosensor entwickelt
Mit ihrem eigens entwickelten, neuartigen „Biosensor“ setzen die Göttinger Herzforscher bei einem wichtigen Botenstoff in den Mikrodomänen der Herzmuskelzellen an: Der Botenstoff cAMP aktiviert bestimmte Proteine, die die Kontraktion der Herzzellen verstärken. Kommt es hier zu Störungen, führt dies zur verminderten Schlagkraft des Herzens und zu Herzrhythmusstörungen. Beide Phänomene führen zu Problemen für Herzschwächepatienten. Über eine Messung der cAMP-Konzentration in den Herzmuskelzellen sind Rückschlüsse über die molekularen Prozesse in den Zellen möglich.
Der neu entwickelte Biosensor ist ein genetisches Konstrukt, das aus zwei Leuchtproteinen mit einer cAMP-Bindestelle in der Mitte besteht. Erhöht sich die cAMP-Konzentration in den Zellen, setzen sich die cAMP-Moleküle an die Bindestelle des Biosensors. Dadurch ändern sich Struktur und Fluoreszenzeigenschaften des Biosensors. Mithilfe von Mikroskopie in hoher subzellularer Auflösung konnten die Wissenschaftler die Mikrodomänen der Herzmuskelzellen erkennen und die Veränderungen in den Zellen messen. Dabei fanden sie heraus, dass bei einer Herzschwäche die Signalleitung in den Herzmuskelzellen von den β1-Rezeptoren in den Membranen hin zu den Mikrodomänen durch das Enzym Phosphodiesterase (PDE) gestört ist. Anders als in gesunden Herzzellen werden die Signale nicht mehr gerichtet zu den mit Calciumpumpen des sarcoplasmatischen Reticulums assoziierten Mikrodomänen transportiert, sondern sie verlaufen deutlich diffuser.
Neue Therapietargets bei Herzschwäche
Bei Herzschwäche ist die Kommunikation zwischen Mikrodomänen und Membranrezeptoren gestört. Um die Herzschwäche zu behandeln, muss die Zellkommunikation wieder hergestellt werden. Das neue Verfahren ermöglicht Einblicke in diese Prozesse und hilft diese zu verstehen. Daraus ergeben sich mögliche Verbesserungen für bereits vorhandene Therapien, wie z.B. die Betablockertherapie oder die Therapie mit Phosphodiesterasen-Hemmer-Therapie (PDE-Hemmer-Therapie). Auch potentielle neue Medikamententargets (Wirkstoff-Zielverbindungen) können nun besser ausgelotet werden. Viele Formen der Phosphodiesterase, einem Enzym, das bei der Herzschwäche eine wichtige Rolle spielt, und deren genaue Wirkweise in Zusammenhang mit den cAMP Mikrodomänen sind noch nicht im kleinsten Detail erforscht. Diese wollen die Forscher als Nächstes genauer untersuchen.
Seit 2012 fördert die Deutsche Forschungsgemeinschaft (DFG) den Sonderforschungsbereich 1002 „Modulatorische Einheiten bei Herzinsuffizienz“ (SFB 1002) unter der Leitung der Universitätsmedizin Göttingen mit über zehn Millionen Euro für zunächst vier Jahre. Ziel des SFB 1002 ist es, innovative Verfahren für die Therapie der Herzinsuffizienz zu entwickeln. Dazu gehören neue Therapien gegen Pumpschwäche und Arrhythmien. Neue Verfahren sollen durch die Identifizierung von spezifischen lokalisierten Therapietargets ermöglicht werden. Im SFB 1002 arbeiten sieben Einrichtungen der Universitätsmedizin Göttingen und das „Max-Planck-Institut für Dynamik und Selbstorganisation“ sowie das „Max-Planck-Institut für Biophysikalische Chemie“ zusammen. Prof. Dr. Gerd Hasenfuß, Direktor der Klinik für Kardiologie und Pneumologie und Vorsitzender des Herzzentrums der Universitätsmedizin Göttingen und des Herzforschungszentrums, ist der Sprecher des SFB 1002.